Распространенные сульфиды и их применение
Введение
Сульфиды уже давно играют важную роль в различных отраслях промышленности. Эти материалы обладают уникальными химическими и физическими свойствами, что позволяет применять их в катализе, хранении энергии, электронике и т. д. В этой статье мы рассмотрим некоторые из наиболее часто используемых сульфидов и их ценные применения.
1. Сульфид лития (Li₂S): Ключевой компонент для хранения энергии
Сульфид лития (Li₂S) является неотъемлемой частью технологии литий-серных (Li-S) батарей - нового решения для хранения энергии с высокой теоретической плотностью энергии. Литий-серные батареи известны тем, что потенциально могут хранить больше энергии, чем традиционные литий-ионные батареи, что делает их перспективными для электромобилей (EV) и сетевых накопителей. Li₂S выступает в качестве катодного материала в Li-S батареях, где его уникальные электрохимические реакции позволяют накапливать и высвобождать энергию.
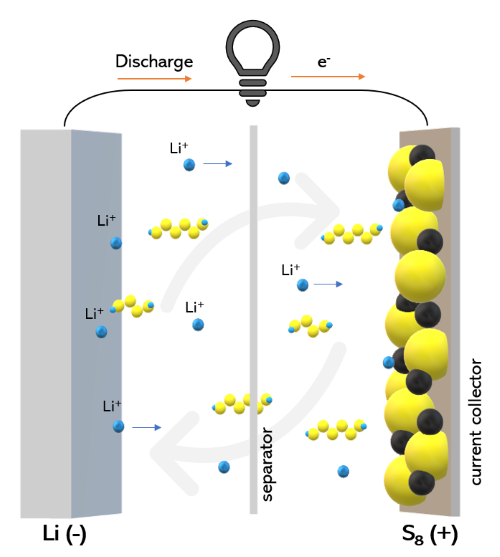 [1]
[1]
Несмотря на свои преимущества, литий-серные батареи сталкиваются с проблемами, включая "эффект шатлинга", когда промежуточные полисульфиды лития растворяются в электролите, сокращая срок службы батареи. Исследователи активно разрабатывают методы стабилизации сульфида лития в батарее, и инновации в этой области приближают литий-серные батареи к коммерческой жизнеспособности.
2. Дисульфид молибдена (MoS₂): Универсальный катализатор и смазочный материал
Дисульфид молибдена (MoS₂) - это, пожалуй, один из самых универсальных сульфидов, который находит применение и как твердая смазка, и как катализатор. В своей природной минеральной форме (молибденит) MoS₂ имеет слоистую структуру, похожую на графит. Такая структура обеспечивает превосходные смазывающие свойства, что делает MoS₂ популярным твердым смазочным материалом в тяжелом машиностроении и аэрокосмических компонентах, где он снижает трение и износ в условиях высоких нагрузок.

Кроме того, MoS₂ служит катализатором при гидрообессеривании- ключевом процессе переработки нефти. В этом процессе MoS₂ удаляет примеси серы из сырой нефти, снижая содержание серы в топливе и тем самым уменьшая выбросы при его сжигании. Каталитические способности MoS₂ обусловлены его активными краевыми участками, которые способствуют реакциям удаления серы. Исследования также изучают его потенциал в качестве катализатора для производства водорода, особенно в реакциях расщепления воды.
3. Сульфиды железа (FeS и FeS₂): Основа металлообработки и не только
Сульфиды железа, включая сульфид железа(II) (FeS) и дисульфид железа (FeS₂, широко известный как пирит или "золото дурака"), широко используются в металлообработке, химическом синтезе и даже в фотовольтаике.
При обработке металлов FeS часто является побочным продуктом, служащим источником серы и железа для дальнейшего использования. Пирит (FeS₂), в свою очередь, используется в производстве серной кислоты - важнейшего промышленного химиката. Диоксид серы (SO₂), образующийся при обжиге пирита, превращается в серную кислоту, которая используется во всех сферах - от производства удобрений до очистки сточных вод.
Кроме того, полупроводниковые свойства FeS₂ позволяют использовать его в качестве фотоэлектрического материала. Природное изобилие пирита и его низкая токсичность делают его привлекательным кандидатом на создание материалов для солнечных батарей. Однако проблемы, связанные со стабильностью и эффективностью преобразования энергии, являются областями, в которых продолжаются исследования.
4. Сульфид цинка (ZnS): Ключевой материал для оптики и люминесцентных приложений
Сульфид цинка (ZnS ) широко используется в оптике и дисплейных технологиях благодаря своей прозрачности в инфракрасном диапазоне и способности излучать свет при возбуждении. Одним из наиболее распространенных применений ZnS является использование в качестве люминофора в экранах дисплеев, светящихся в темноте материалах и рентгеновских экранах. При легировании небольшим количеством меди люминофоры ZnS излучают свет, который можно настраивать для различных применений, создавая дисплеи, которые остаются яркими и энергоэффективными.
Помимо оптических применений, ZnS также играет роль в производстве инфракрасной оптики, например линз и окон. Поскольку ZnS прозрачен как в видимом, так и в инфракрасном спектре, он является идеальным выбором для этих применений, особенно в технологиях ночного видения и тепловидения.
5. Сульфид кадмия (CdS): Применение в фотовольтаике и электронике
Сульфид кадмия (CdS) - еще один важный полупроводниковый материал, используемый в основном в фотогальванических элементах и различных электронных приложениях. В солнечных батареях CdS часто используется в паре с теллуридом кадмия (CdTe) для создания высокоэффективного фотоэлектрического слоя. Свойства CdS позволяют ему эффективно поглощать солнечный свет, что делает его важным компонентом в тонкопленочных солнечных батареях.
Однако кадмий - токсичный элемент, и опасения по поводу воздействия на окружающую среду привели к постоянным исследованиям более безопасных альтернатив. Тем не менее тонкопленочные солнечные технологии на основе CdS остаются конкурентоспособными благодаря высокой эффективности, простоте производства и масштабируемости, что стимулирует дальнейшее совершенствование их конструкции для решения экологических проблем.
6. Сульфид никеля (NiS): Катализатор в химической промышленности
Сульфид никеля (NiS) играет важную роль в качестве катализатора в химических процессах, особенно в гидрогенизации органических соединений. NiS может катализировать реакции, в результате которых водород присоединяется к органическим молекулам, что важно для производства всего - от маргарина до некоторых фармацевтических препаратов. Стабильность материала в жестких условиях реакции делает его эффективным и долговечным катализатором.
Сульфид никеля также находит применение в некоторых специальных стеклах и керамике. В производстве стекла частицы NiS известны тем, что они вызывают "спонтанное разрушение" закаленного стекла, и производители стремятся лучше понять эту область, чтобы минимизировать подобные случаи. Хотя это относительно нишевое применение, оно подчеркивает важность химического поведения NiS и его последствий для различных материалов.
7. Сульфид меди(I) (Cu₂S): Проводящие пленки и антибактериальное применение
Сульфид меди(I) (Cu₂S) используется в электронной промышленности в качестве проводящего материала в тонких пленках. Пленки Cu₂S обладают высокой электропроводностью, что делает их пригодными для использования в электронных устройствах, особенно в областях, требующих прозрачных проводящих пленок, таких как сенсорные экраны и другие дисплейные технологии.
Cu₂S также обладает антимикробными свойствами, что особенно полезно в медицинских устройствах и покрытиях, где важна устойчивость к бактериям. Исследователи изучают потенциал наночастиц сульфида меди в качестве антимикробных агентов, особенно в сфере здравоохранения, где они могут помочь уменьшить количество инфекций и улучшить результаты лечения пациентов.
|
Сульфид |
Области применения |
Ключевые свойства |
|
литий-серные батареи для электромобилей и хранения |
Высокая энергетическая плотность, перезаряжаемые |
|
|
Смазка в машиностроении, катализатор для очистка топлива |
Уменьшает трение, стабильный катализатор |
|
|
Сульфиды железа |
Обработка металлов, серная кислота, солнечные батареи |
Обеспечивает серу, полупроводник |
|
Дисплеи, инфракрасная оптика, светящиеся материалы |
Инфракрасный прозрачный, люминесцентные |
|
|
Сульфид кадмия |
Солнечные элементы, электроника |
Светопоглощающие, в паре с CdTe |
|
Сульфид никеля |
Химический катализатор, стеклокерамика |
Стабилен в реакциях, влияет на закаленное стекло |
|
Сульфид меди(I) |
Проводящие пленки, антибактериальные покрытия |
Высокая проводимость, антимикробные |
Заключение
Сернистые материалы предлагают удивительный спектр применений. От хранения энергии и катализа до электроники и оптики - сульфиды являются неотъемлемой частью многих передовых технологий и промышленных процессов. Инновации в аккумуляторных технологиях, катализе, фотовольтаике и других областях продолжают использовать возможности этих соединений, повышая эффективность и расширяя сферу их применения. Более подробную информацию вы можете получить в Stanford Advanced Materials (SAM).
Ссылки:
[1] Литий-серная батарея. (2023, 20 августа). В Википедии. https://en.wikipedia.org/wiki/Lithium%E2%80%93sulfur_battery

 Бары
Бары
 Бисер и шары
Бисер и шары
 Болты и гайки
Болты и гайки
 Кристаллы
Кристаллы
 Диски
Диски
 Волокна и ткани
Волокна и ткани
 Фильмы
Фильмы
 Хлопья
Хлопья
 Пены
Пены
 Фольга
Фольга
 Гранулы
Гранулы
 Медовые соты
Медовые соты
 Чернила
Чернила
 Ламинат
Ламинат
 Шишки
Шишки
 Сетки
Сетки
 Металлизированная пленка
Металлизированная пленка
 Тарелка
Тарелка
 Порошки
Порошки
 Род
Род
 Простыни
Простыни
 Одиночные кристаллы
Одиночные кристаллы
 Мишень для напыления
Мишень для напыления
 Трубки
Трубки
 Стиральная машина
Стиральная машина
 Провода
Провода
 Конвертеры и калькуляторы
Конвертеры и калькуляторы





 Chin Trento
Chin Trento



